Bacteris PAO1 infectant el peix zebra amb la mutació en el promotor de nrdD (panell superior, menys verd) i amb un cep amb la mutació corregida com en els aïllats clínics (panell inferior, molt més verd).
Aquesta recerca, finançada parcialment per la Fundació Española de Fibrosi Quística i per Obra Social “la Caixa”, i duta a terme per Eduard Torrents, investigador principal al’IBEC i l’estudiant de doctorat Anna Crespo, estudia noves estratègies per combatre les infeccions bacterianes basant-se en l’ús del cep PAO1 del bacteri Pseudomonas aeruginosa, la qual s’empra com a referència en la majoria dels laboratoris clínics i de recerca
Un enzim essencial per a la divisió cel·lular de la PAO1 és la ribonucleòtid reductasa RNR, que subministra els monòmers necessaris per a la síntesi i reparació de l’ADN. P. aeruginosa és un dels pocs microorganismes que codifica tres classes diferents de RNR en el seu genoma, la qual cosa li permet créixer i adaptar-se a diverses condicions ambientals, fins i tot durant la infecció, raó per la qual s’ha tornat tan omnipresent en els laboratoris de microbiologia.
Els investigadors van descobrir que l’absència d’activitat de la RNR condueix a l’elongació cel·lular en el cep PAO1, la qual cosa indica falta de creixement. A més, l’expressió gènica de la RNR durant la anaerobiosis – processos que ocorren en absència d’oxigen – difereix entre els ceps clínics de P. aeruginosa i els emprats al laboratori, doncs la RNR de classe III s’expressa molt més en aïllats clínics de P. aeruginosa en comparació del cep de laboratori.
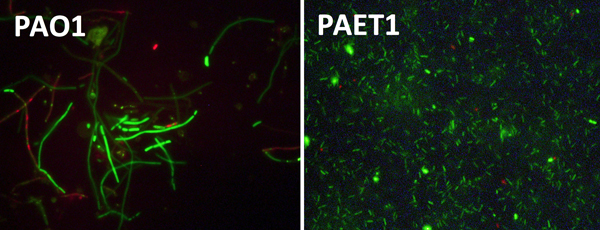
Les cèl·lules bacterianes del cep PAO1 (esquerra) i cèl·lules d’un aïllat clínic (dreta) crescudes en absència d’oxigen. El cep PAO1 mostra clars defectes de creixement, amb cèl·lules allargades en comparació de l’aïllat clínic.
“Sembla que PAO1 s’ha adaptat a les condicions de laboratori, una mica com quan els nostres cossos es tornen resistents als antibiòtics”, diu Eduard. “Durant la infecció, la P. aeruginosa clínica actua en condicions on l’oxigen no està present, però el cep de laboratori PAO1 de P. aeruginosa no pot créixer de la mateixa manera sota aquestes condicions. En aquest treball s’ha identificat que una sola mutació a la regió promotora de la RNR de classe III del cep PAO1 interromp la seva transcripció anaeròbica, disminuint la seva virulència. Això significa que PAO1 no és el cep adequat per a la recerca en condicions anaeròbiques o d’infecció, ni per a la cerca de nous compostos antimicrobians.
El descobriment es va fer mentre l’Eduard desenvolupava noves estratègies per combatre infeccions bacterianes i possibles dianes terapèutiques, la qual cosa està fortament relacionada amb la fibrosis quística. Aquesta malaltia provoca la formació i acumulació de moc espès en els pulmons, els intestins, el pàncrees i el fetge, i els pacients pateixen insuficiència respiratòria a causa de la colonització bacteriana crònica (biopel·lícules) als pulmons. La recerca de l’Eduard està prenent un nou enfocament per superar aquest problema, desenvolupant sistemes al laboratori que imiten els pulmons d’un pacient, i també introduint diverses estratègies de nanomedicina per combatre aquestes infeccions.
A finals de 2016, el grup va rebre un generós impuls estès al llarg de tres anys gràcies a una nova iniciativa de finançament d’Obra Social “La Caixa”, que va fer possible el triangle de cooperació actual entre els investigadors, la clínica i les associacions de pacients.
—
Article referenciat: Anna Crespo, Joan Gavaldà, Esther Julián & Eduard Torrents (2017). “A single point mutation in class III ribonucleotide reductase promoter renders Pseudomonas aeruginosa PAO1 inefficient for anaerobic growth and infection”. Scientific Reports, 7, Article number: 13350





